薬事申請関連文書ライティング
- 総括報告書(CSR):臨床
- コモン・テクニカル・ドキュメント(CTD):非臨床/臨床
- 照会事項回答対応
- その他(有害事象の叙述の作成、プロトコル、ICFのレビュー等)
投稿論文ライティング
- 総説(病態、治療法、臨床成績)
- 臨床試験(RCT、観察研究、症例報告、レトロ研究、PMS)
- 非臨床(毒性、薬物動態、薬理)
- 調査(アンケート調査、WEB調査)
投稿ターゲット雑誌の投稿規程調査、骨子作成、英文校正、投稿支援、レビュー対応を含め、論文投稿に関するすべてのプロセスをサポートいたします。
QC
- 英文/和文の各種文書の整合性チェック
- 英文/和文の各種文書の妥当性チェック
- フォーマットチェック
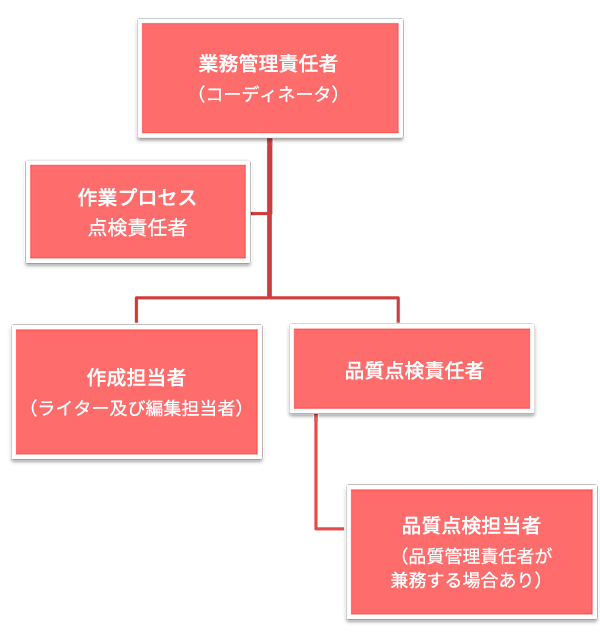
プロジェクト・マネージメント体制
| 担当者 | 責務 |
|---|---|
| 業務管理責任者 (コーディネータ) | 当該業務において関連資料の受領から成果物納品までの責任を負う。 当該業務を担当する各担当者を指名し、業務が円滑に実施されているか、進捗管理を行う。また、資料授受及び納品を行う。 |
| 作成担当者 (ライター及び編集担当者) | 作成文書案の作成及び編集作業を担当する。 |
| 品質点検責任者 | 品質点検担当者が実施した品質点検結果(出力した作成文書案にチェック、指摘及び疑義事項を記入した原稿)について品質点検の内容が間違いなく、抜けなく記載されているか確認を行う。 また当該業務に関する品質点検業務の責任を負う。 |
| 品質点検担当者 | 作成担当者により作成された作成文書案の品質点検業務を行う。提供資料の内容と合致しているか、事前に確認した指示事項に合っているか、また全体の整合性がとれているかをチェックリスト等をもとに確認する。 |
| 作業プロセス点検責任者 | 当該業務が事前に合意した手順(関連する手順書等)通りに遂行されたかどうか、点検を行う。 |
主な受託実績
- 製薬・医療機器企業等:30社以上
- CRO・翻訳会社等:8社
- 大学 :4施設