安全性情報管理業務の受託
経験、ノウハウを生かし、安全管理業務を支援いたします
ウィズウィグでは1998年より安全性情報に関わる業務を受託しており、当初はMS-WORD等によるCIOMS、規制当局報告様式の作成業務から安全性情報に携わってまいりました。長年にわたる経験とノウハウ、また人材資源を生かし、お客様の安全性情報管理業務を支援いたします。
ご要望に応じた業務体制を構築いたします
ウィズウィグでは、治験から市販に至るステージにおいて、小規模なプロジェクトから数十人単位という中・大規模なプロジェクトまで対応が可能です。
オンサイト(受託先企業内での業務)、オフサイト(弊社内での業務)のいずれの業務体制もご要望に合わせ構築させていただきます。例えば、オンサイトに数名が常駐し、受付対応や症例ファイリング、進捗管理を行い、入力および翻訳はオフサイトで行うといった柔軟な対応も可能です。
安全性情報翻訳
医学的に正確、かつ期限厳守にて症例翻訳をお請けしております
お客様が入手した安全性情報を評価するための、症例経過、医師コメント等の翻訳を、正確に、かつHeadquartersや海外提携会社の報告期限を遵守するスピードでご提供しております。
ウィズウィグでは、報告書に記載してある情報(症例経過や医師コメント)を、評価ご担当者が判断を誤らないよう適切な用語選択と記載ルールを守り、背景情報との齟齬がない、医学的に正確な翻訳を納品するよう心がけております。
また、EDCにて施設が直接英文で症例経過、コメント等を報告するための症例英訳のサービスもご提供しております。弊社が治験施設に直接翻訳サービスをご提供することにより、治験依頼者(製薬企業様、医療機器企業様)の意思が介在しないフローを構築しております。
安全性情報管理業務で必要となる各種文書・様式の翻訳及び作成をお請けしております
国内および海外規制当局報告様式案作成をはじめとして、Headquartersや海外提携先等への指定報告様式案(CIOMS形式等)作成、症例叙述・各種ラインリスト案作成、添付文書、文献等、安全性情報管理業務で必要となる各種文書の翻訳および資料作成をお請けしております。
医薬・科学技術専門の翻訳会社として培ってきた経験やノウハウ、人的資源に加え、約20年にわたる安全性情報業務支援の経験、社内専門家の医薬に関する専門知識をもとに、迅速かつ高品質な翻訳を提供しております。
文献スクリーニング
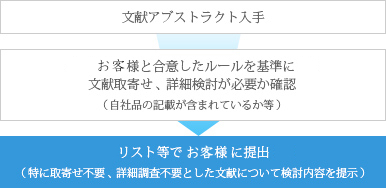
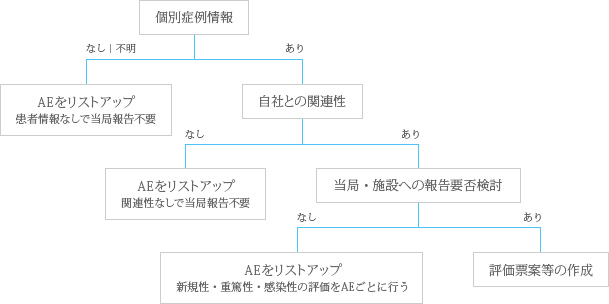
ウィズウィグでは、お客様の入手文献情報から規制当局報告要否判断までにおける評価支援業務をご提供いたします。
文献記載中に報告すべき情報(副作用報告・研究報告)が含まれているか否かを、お客様との間で取り決めた一定のルールに従ってスクリーニングいたします。